Kontakt:Fehler Zhou (Herr.)
Tel: plus 86-551-65523315
Handy/WhatsApp: plus 86 17705606359
Frage:196299583
Skype:lucytoday@hotmail.com
Email:sales@homesunshinepharma.com
Hinzufügen:1002, Huanmao Gebäude, Nr.105, Mengcheng Straße, Hefei Stadt, 230061, China
Sol-Gel Technologies gab kürzlich bekannt, dass die US-amerikanische Food and Drug Administration (FDA) ihr erstes patentiertes Arzneimittelprodukt Twyneo (Tretinoin/Benzoylperoxid, 0,1%/3%) Creme zugelassen hat, die täglich eine topische Anwendung zur Behandlung von Akne vulgaris ist (Akne vulgaris) bei pädiatrischen Patienten und erwachsenen Patienten ab 9 Jahren.
Twyneo ist eine topische Creme, die 0,1% Tretinoin (Retinsäure) und 3% Benzoylperoxid enthält. Es ist erwähnenswert, dass Twyneo das erste von der US-amerikanischen FDA zugelassene Kombinationsprodukt ist, das eine feste Dosis von Tretinoin und Benzoylperoxid enthält. Tretinoin und Benzoylperoxid werden häufig bei der Behandlung von Akne vulgaris verwendet; Benzoylperoxid kann jedoch einen Abbau des Tretinoin-Moleküls verursachen, so dass bei gleichzeitiger oder kombinierter Verwendung in derselben Formel seine Wirksamkeit verringert werden kann.
Twyneo verwendet die proprietäre Technologie von Sol-Gel, um Tretinoin und Benzoylperoxid in Mikrokapseln auf Siliziumbasis einzubetten, um das Tretinoin vor dem Abbau durch Benzoylperoxid zu stabilisieren und es langsam im Laufe der Zeit freizusetzen. Eine Art pharmazeutischer Wirkstoffe, die eine gute Wirksamkeit und Sicherheit bieten. Die Formel von Twyneo verwendet eine Kieselsäure-Kern-Schale-Struktur, um Retinsäurekristalle und Benzoylperoxid-Kristalle zu mikroverkapseln, sodass diese beiden Wirkstoffe in der Creme enthalten sind. Twyneo's Patentschutzzeit läuft bis 2038.

Twyneo pharmazeutische Wirkstoffe und Sol-Gel's Drug Delivery-Technologie
Sol-Gel hat sich mit Galderma zusammengetan, um Twyneo in den USA zu vermarkten. Als Reaktion auf diese Genehmigung erhält Sol-Gel eine behördliche Meilensteinzahlung und behält sich die Option vor, die US-Vermarktungsrechte fünf Jahre nach der ersten Vermarktung in den USA zurückzuerhalten.
Twyneo's New Drug Application (NDA) wurde am 26. Juli 2021 von der US-amerikanischen FDA genehmigt ). Die Daten zeigen, dass Twyneo bei der Behandlung von Akne vulgaris im Gesicht bei Menschen ab 9 Jahren Wirksamkeit und gute Verträglichkeit gezeigt hat.
Akne vulgaris ist eine häufige multifaktorielle Hauterkrankung. Nach Angaben der American Academy of Dermatology (AAS) sind in den Vereinigten Staaten bis zu 50 Millionen Menschen von der Krankheit betroffen. Die Krankheit tritt am häufigsten im Kindes- und Jugendalter auf (betrifft 80-85% der Jugendlichen), kann aber auch bei Erwachsenen auftreten. Patienten mit Akne vulgaris haben Läsionen im Gesicht, auf der Brust, am Hals und am Rücken des Körpers, die viele fettige Drüsen enthalten. Diese Läsionen können entzündet (Papeln, Pusteln, Knötchen) oder nicht entzündet (Akne) sein. Akne vulgaris kann die Lebensqualität von Patienten stark beeinträchtigen. Neben dem enormen Risiko bleibender Narben im Gesicht kann das Auftreten von Läsionen auch zu psychischen Anspannungen, sozialem Rückzug und vermindertem Selbstwertgefühl führen.
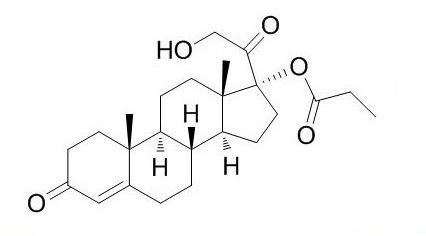
Die molekulare Struktur des Winlevi-Wirkstoffs Clascoteron
Erst kürzlich gaben Sun Pharmaceuticals und Cassiopea SpA bekannt, dass sie das Akne-Medikament Winlevi (Clascoteron 1%, Creme) im vierten Quartal 2021 auf den US-Markt bringen werden. Winlevi wurde im August 2020 von der US-amerikanischen FDA zugelassen. Es ist ein neues Art von Arzneimittel mit einem einzigartigen Wirkmechanismus. Als topisches Medikament wird es zur Behandlung von Akne vulgaris (Akne vulgaris) bei Patienten ab 12 Jahren angewendet. Akne ist die häufigste Hautkrankheit in den Vereinigten Staaten, von der jedes Jahr 50 Millionen Menschen betroffen sind, aber die FDA hat vor fast 40 Jahren zuletzt ein Akne-Medikament mit einem neuen Wirkmechanismus (MOA) zugelassen.
Winlevi (Clascoteron 1%, Creme) ist das erste Akne-Medikament mit einem neuen Wirkmechanismus (MOA), das in den letzten 40 Jahren von der US-amerikanischen FDA zugelassen wurde und Dermatologen und Patienten eine neue und wirksame Behandlungsmethode bieten wird. Im Gegensatz zu oralen Hormonen zur Behandlung von Akne kann Winlevi sowohl bei männlichen als auch bei weiblichen Patienten angewendet werden.
Der pharmazeutische Wirkstoff von Winlevi ist Clascoteron, ein erstklassiger topischer Androgenrezeptor-Inhibitor, der entwickelt wurde, um die Androgenkomponente der männlichen und weiblichen Akne zu lösen. Die Rolle von Androgenrezeptorhemmern besteht darin, die entzündlichen Wirkungen dieser Hormone zu begrenzen, um die Talgsekretion zu erhöhen. Clascoteron ist ein niedermolekulares Medikament, das die Haut durchdringen kann, um die Androgenrezeptoren in den Talgdrüsen und Haarfollikeln zu erreichen. Dieses Medikament ist die erste sichere und wirksame topische Androgen-Inhibitor-Therapie ohne systemische Nebenwirkungen.
Winlevi verwendet zweimal täglich topische Medikamente, um auf den Androgenrezeptor an der Medikationsstelle einzuwirken, um die lokale (Haut-)Wirkung von Dihydrotestosteron (DHT) zu hemmen. DHT ist ein wichtiger treibender Faktor für das Auftreten von Akneläsionen. Laborstudien haben gezeigt, dass Clascoteron die Lipidproduktion in ölproduzierenden Zellen (Sebcyten) hemmen und entzündungsfördernde Zytokine und Mediatoren reduzieren kann, die von Androgenen beeinflusst werden. Daher wird der Weg, der das Auftreten von Akneläsionen fördert, durch Clascoteron zerstört.
Daten aus zwei wichtigen klinischen Phase-3-Studien zeigten, dass Winlevi statistisch hochsignifikante Verbesserungen bei allen primären klinischen Endpunkten zeigte, was die erfolgreiche Behandlung von Akne und die Verringerung von Akneläsionen belegt und bei zweimal täglicher Anwendung gut vertragen wurde. Die häufigste lokale Hautreaktion ist ein leichtes Erythem. Während der Studie wurden keine schwerwiegenden Nebenwirkungen im Zusammenhang mit der Behandlung aufgezeichnet; lokale Hautreaktionen (sofern vorhanden) waren ähnlich wie bei sonstigen Bestandteilen, überwiegend mild. Die Sicherheit des Arzneimittels wurde in einer offenen Sicherheitsstudie bestätigt, bei der die Oberfläche des Arzneimittels auf Gesicht und Rumpf ausgedehnt wurde. Die verlängerte topische Anwendungszeit und -abdeckung erhöhte das Auftreten von signifikanten Nebenwirkungen nicht.