Kontakt:Fehler Zhou (Herr.)
Tel: plus 86-551-65523315
Handy/WhatsApp: plus 86 17705606359
Frage:196299583
Skype:lucytoday@hotmail.com
Email:sales@homesunshinepharma.com
Hinzufügen:1002, Huanmao Gebäude, Nr.105, Mengcheng Straße, Hefei Stadt, 230061, China
Merck KGaA gab kürzlich bekannt, dass die US Food and Drug Administration (FDA) das gezielte Krebsmedikament Tepmetko (Tepotinib) zugelassen hat, das ein hochselektiver, einmal täglich erwerdender oraler MET-Hemmer zur Behandlung von erwachsenen Patienten mit fortgeschrittenem nicht-kleinzelligem Lungenkrebs (NSCLC) ist, das das MET-Exon 14-Skipping-Änderung (METex14 skipping) trägt. Tepmetko erhielt eine vorrangige Überprüfung und beschleunigte Zulassung durch das FDA Real-Time Oncology Review (RTOR) Pilotprogramm. Die Zulassung basiert auf Daten über die Gesamtansprechrate und die Dauer der Ansprechzeit, und die weitere Zulassung für diese Indikation hängt von der Überprüfung und Beschreibung des klinischen Nutzens in Bestätigungsstudien ab.
Im März 2020 erhielt Tepmetko in Japan die weltweit erste zulassungstechnische Zulassung für die Behandlung von Patienten mit nicht resezierbarem, fortgeschrittenem oder wiederkehrendem NSCLC, die Änderungen in METex14 übersprungen haben. Im November 2020 nahm die Europäische Arzneimittel-Agentur (EMA) teppetkos Antrag an und leitete den Überprüfungsprozess ein.
Es ist erwähnenswert, dass Teppetko der weltweit erste orale MET-Hemmer ist, der für die Behandlung fortgeschrittener NSCLC-Patienten mit MET-genetischen Veränderungen zugelassen ist. In Japan wurde Teppetko die Orphan Drug Designation (ODD) und die SAKIGAKE Designation (Innovative Drug) verliehen. In den Vereinigten Staaten wurde Teppetko Orphan Drug Designation (ODD) und Breakthrough Drug Designation (BTD) verliehen.
Tepmetko ist auch der erste und einzige MET-Hemmer, der von der US FDA für die Behandlung von Patienten mit METex14 übersprungenem metastasierendem NSCLC zugelassen wurde. Im September 2020 wurde das gezielte Krebsmedikament Tabrecta (Capmatinib) von Novartis zugelassen, das als erster von der FDA zugelassener MET-Hemmer zur Behandlung erwachsener Patienten mit METex14-Überspringen von Veränderungen des metastasierenden NSCLC zugelassen wurde.
Sowohl Tepmetko als auch Tabrecta sind für die Anwendung bei Patienten zugelassen, die zuvor keine Behandlung erhalten haben (First-Line) und Patienten, die zuvor behandelt (behandelt) wurden. In Bezug auf Medikamente, Tepmekto wird einmal täglich oral eingenommen, und Tabrecta wird oral zweimal täglich eingenommen.
Die zulassungsrechtliche Zulassung von Tepmetko basiert auf Daten aus der entscheidenden Phase-II-STUDIE Phase II VISION (NCT02864992). Dies ist die bisher größte klinische Studie, die an metastasierenden NSCLC-Patienten mit METex14-Überspringen-Änderungen durchgeführt wurde. Insgesamt 152 NSCLC-Patienten mit METex-Skip-Änderungen erhielten eine Tepmetko-Behandlung.
Die Ergebnisse zeigten, dass Teppetko eine Gesamtansprechrate (ORR) von 43% bei Patienten hatte, die zuvor keine Behandlung erhalten hatten (n=69, Erstbehandlungsgruppe) und zuvor behandelte Patienten (n=83, behandelte Gruppe). 99%CI: 32-56) und 43% (95%CI: 33-55), die mediane Ansprechdauer (DOR) der beiden Gruppen betrug 10,8 Monate und 11,1 Monate, und die Ansprechzeit der beiden Gruppen betrug ≥ 6 Monaten Der Anteil der Patienten betrug 67% bzw. 75%, und der Anteil der Patienten mit Remissionszeit ≥ 9 Monaten betrug 30% bzw. 50%.
Zur sicheren Population gehörten 255 Patienten mit METex14 skip change positive NSCLC, die Tepmetko-Behandlung in der VISION-Studie erhielten. 1 Fall (0,4%) starb an Lungenentzündung, 1 Fall (0,4%) an Leberversagen gestorben ist, und 1 Fall (0,4%) an Dyspnoe durch übermäßige Flüssigkeit verursacht. Schwere Nebenwirkungen traten bei 45% der mit Tepmetko behandelten Patienten auf. Schwere Nebenwirkungen mit einer Inzidenz von > 2%, einschließlich Pleuraerguss (7%), Lungenentzündung (5%), Ödeme (3,9%), Dyspnoe (3,9%), Verschlechterung der allgemeinen Gesundheit (3,5%), Lungenembolie (2 %) und Muskel-Skelett-Schmerzen (2%). Die häufigsten Nebenwirkungen (≥20%) bei Patienten, die Teppetko einnehmen, sind Ödeme, Müdigkeit, Übelkeit, Durchfall, Muskel-Skelett-Schmerzen und Atembeschwerden.
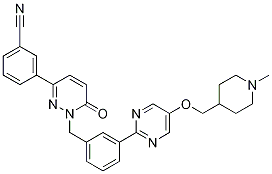
Molekulare Struktur von Tepotinib (Bildquelle: chemicalbook.com)
Weltweit ist Lungenkrebs mit 2 Millionen Diagnosen und 1,7 Millionen Todesfällen pro Jahr die häufigste Krebsart und die häufigste Ursache für Krebstode. Derzeit wurden bei vielen Krebsarten drei MET-Signalwegänderungen (einschließlich METex14-Sprungänderungen, MET-Amplifikation und MET-Protein-Überexpression) entdeckt, die mit tumoraggressivem Verhalten und schlechter klinischer Prognose zusammenhängen. Es wird geschätzt, dass Veränderungen des MET-Signalwegs in 3-5% der NSCLC-Fälle auftreten.
Tepotinib ist ein oraler MET-Kinase-Inhibitor bei Merck, der die onkogenen Signale, die durch MET-Änderungen (Gen) verursacht werden, stark und hochselektiv hemmen kann, einschließlich METex14-Sprungänderungen, MET-Amplifikation und MET-Protein-Überexpression. , Hat das Potenzial, die Prognose von aggressiven Tumorpatienten mit diesen spezifischen MET-Änderungen zu verbessern. Neben NSCLC evaluiert Merck auch aktiv Tepotinib in Kombination mit neuen Therapien für andere Tumorindikationen.
Im September 2019 erteilte die US FDA Tepotinib Breakthrough Drug Designation (BTD) zur Behandlung von Patienten mit metastasierendem NSCLC, die nach einer platinhaltigen Chemotherapie Fortschritte gemacht haben und METex14 Sprungänderungen tragen.
Derzeit führt Merck auch eine weitere Studie INSIGHT 2 (NCT03940703) durch, um die Kombination von Tepotinib und Tyrosinkinase-Inhibitor (TKI)-Osimertinib für EGFR-Mutationen und METs zu bewerten, die Resistenzen gegen zuvor akzeptierte EGFR-TKIs erworben haben. Patienten mit erweitertem, lokal fortgeschrittenem oder metastasierendem NSCLC.