Kontakt:Fehler Zhou (Herr.)
Tel: plus 86-551-65523315
Handy/WhatsApp: plus 86 17705606359
Frage:196299583
Skype:lucytoday@hotmail.com
Email:sales@homesunshinepharma.com
Hinzufügen:1002, Huanmao Gebäude, Nr.105, Mengcheng Straße, Hefei Stadt, 230061, China
Fennec Pharmaceuticals gab kürzlich bekannt, dass es bei der US-amerikanischen Food and Drug Administration (FDA) einen neuen Arzneimittelantrag (NDA) für Pedmark (eine einzigartige Formulierung von Natriumthiosulfat) eingereicht hat, das bei pädiatrischen Patienten zur Vorbeugung einer platinhaltigen Chemotherapie eingesetzt wird. Ototoxizität, insbesondere: bei Patienten mit begrenzten, nicht metastasierten soliden Tumoren im Alter von 1 Monat bis 18 Jahren, um eine durch eine Cisplatin-Chemotherapie verursachte Ototoxizität zu verhindern.
Nach Erhalt des letzten Protokolls des Klasse-A-Meetings mit der FDA legte Pedmark NDA es erneut vor. Es ist wichtig, dass in dem am 10. August 2020 eingegangenen vollständigen Antwortschreiben (CRL) die Mängel der Einrichtungen des Arzneimittelherstellers erwähnt wurden, aber keine klinischen Sicherheits- oder Wirksamkeitsprobleme festgestellt wurden und keine weiteren klinischen Daten erforderlich waren.
Pedmark ist ein Prüfpräparat, bei dem es sich um eine wasserlösliche Thiolverbindung handelt, die als chemisches Reduktionsmittel verwendet wird. Eine längere Verabreichung (4-8 Stunden) und hochdosiertes Pedmark (16-20 g/m2) können Tiermodelle und Patienten vor Immunität schützen. Ototoxizität durch Platin.
Im Falle einer Zulassung wird Pedmark das erste Produkt sein, das Hörverlust bei Kindern durch Cisplatin verhindert. Zuvor hat die FDA Pedmark Orphan Drug Designation, Fast Track Designation und Breakthrough Drug Designation verliehen. Derzeit wird das Medikament (europäischer Handelsname: Pedmarqsi) auch von der Europäischen Arzneimittelagentur (EMA) geprüft.
Rosty Raykov, CEO von Fennec Pharmaceuticals, sagte:"Wir freuen uns, die NDA für Pedmark erneut vorzulegen. Wir freuen uns auf die Zusammenarbeit mit der FDA während des Überprüfungsprozesses. Wir setzen uns weiterhin dafür ein, das Risiko eines lebenslangen Hörverlusts bei Kindern, die eine Cisplatin-Chemotherapie erhalten, zu reduzieren. Mit der Zulassung wird Pedmark die erste von der FDA zugelassene Therapie sein, die das Risiko einer Cisplatin-induzierten Ototoxizität bei Kindern verringert.&Zitat;
Cisplatin und andere Platinverbindungen sind die grundlegenden Chemotherapeutika für viele bösartige Erkrankungen im Kindesalter. Leider kann eine Behandlung auf Platinbasis zu Ototoxizität oder Hörverlust führen, der dauerhaft, irreversibel und besonders schädlich für Überlebende von Krebs im Kindesalter ist.
In den Vereinigten Staaten und Europa erhalten schätzungsweise mehr als 10.000 Kinder jährlich eine platinbasierte Chemotherapie. Unter ihnen haben 40%-90% der Kinder eine schwere und irreversible Ototoxizität. Die Häufigkeit von Ototoxizität bei diesen Kindern hängt von der Dosis und der Dauer der Chemotherapie ab, und viele dieser Kinder benötigen lebenslange Hörgeräte. Derzeit gibt es keine Medikamente, die diesen Hörverlust verhindern können. Nur teure, technisch schwierige, suboptimale Cochlea-Implantate (Innenohr)-Implantate haben sich als gewisse Vorteile erwiesen. Bei Patienten mit Ototoxizität im kritischen Entwicklungsstadium fehlt es Säuglingen und Kleinkindern an Sprech- und Sprachentwicklung sowie Lese- und Schreibfähigkeiten, und älteren Kindern und Jugendlichen mangelt es an sozialer und emotionaler Entwicklung und pädagogischen Leistungen.
Pedmark wurde von einem kooperativen Team in 2 klinischen Phase-III-Studien zur Vorbeugung und Verringerung von Ototoxizität bewertet, darunter die COG ACCL0431-Studie und die SIOEL-6-Studie. Beide Studien wurden erfolgreich abgeschlossen. Die Studie COG ACCL0431 umfasste 5 Arten von Krebs im Kindesalter. Diese Krebsarten werden normalerweise mit einer intensiven Cisplatin-Chemotherapie behandelt, um lokalisierte und disseminierte Krankheiten zu behandeln, einschließlich neu diagnostizierter Hepatoblastome, Keimzelltumoren, Osteosarkomen, Neuroblastome und Medullazelltumoren. In die SIOPEL-6-Studie wurden nur Patienten mit Hepatoblastom mit lokalisierten Tumoren eingeschlossen.
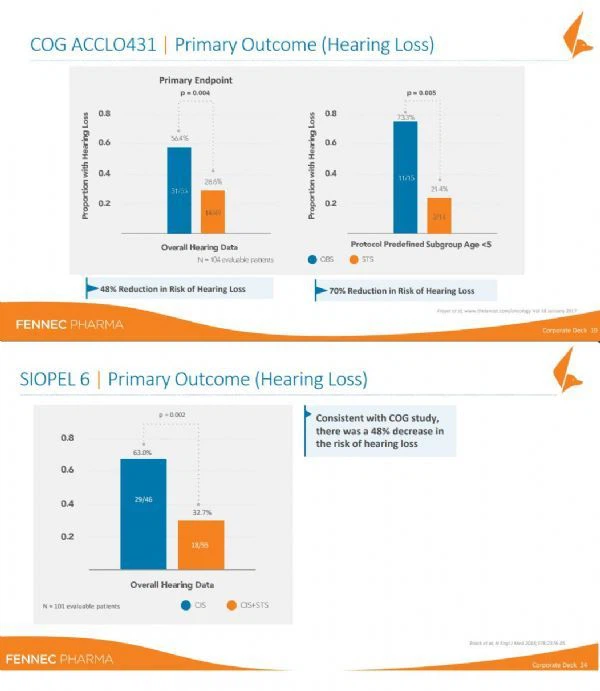
Daten aus klinischen Pedmark-Studien
Pedmark kann Zellen auf verschiedene Weise vor Platintoxizität schützen. Diese chemischen Schutzmechanismen schließen sich nicht gegenseitig aus. Pedmark kann Platinkomplexe inaktivieren und sie ohne Zytotoxizität kovalent an Thiole binden. Obwohl eine große Menge an freiem Platin im Blutkreislauf nach 4 Stunden der Platinverabreichung verschwand, war der Schutz von Pedmark&gegen platinbedingten Hörverlust auch nach 8 Stunden verzögerter Platinverabreichung wirksam. Dies weist darauf hin, dass Pedmark an den Platin/Protein-Komplex binden kann, wodurch dessen Toxizität minimiert wird. Ein möglicher Mechanismus, bei dem Platin zu Hörverlust führt, ist auf die Ablagerung von proteingebundenem Platin in der Cochlea zurückzuführen.
Der andere Mechanismus von Pedmark zum Schutz der Ototoxizität besteht darin, reaktive Sauerstoffspezies (ROS) zu entfernen und den Gehalt an endogenen Reduktionsmitteln (wie GSH) zu erhöhen. Im Innenohr kann die Cochlea Pedmark in Perilymphe oder Endolymphe konzentrieren und den chemischen Schutz von Pedmark&vor Ototoxizität lokal verbessern. Daher wird die Cisplatin-vermittelte (über ROS) Haarzellapoptose durch die reduzierenden Eigenschaften von Natriumthiosulfat (STS) behindert.